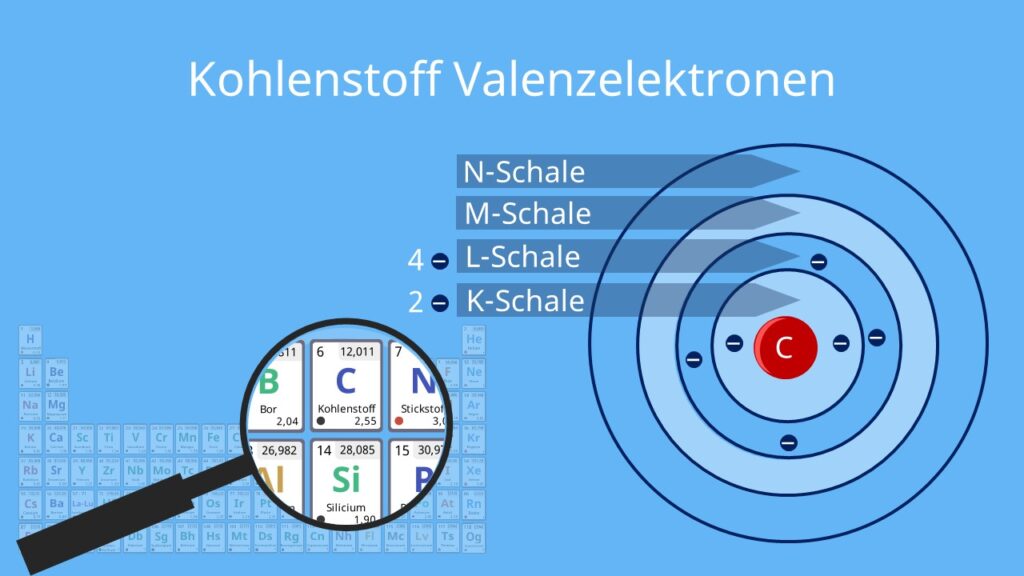
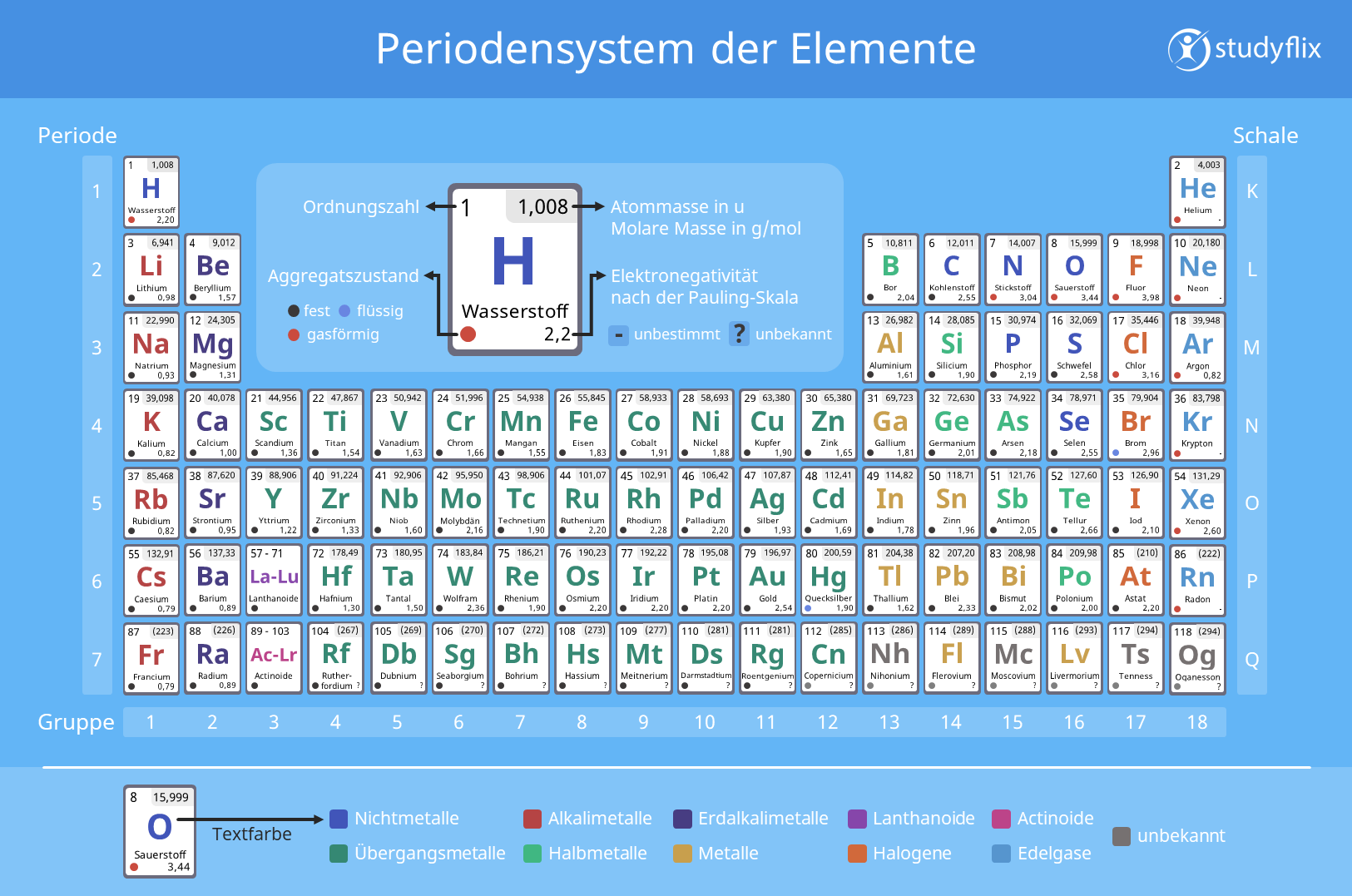
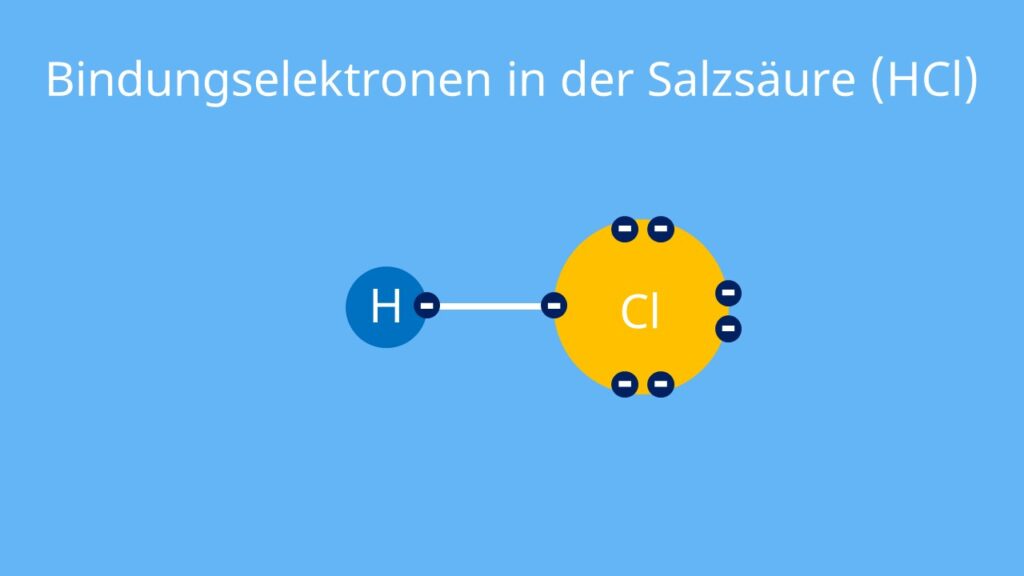
Für die chemischen Elemente in den Hauptgruppen gilt, dass die Nummer der Hauptgruppe dir die Anzahl der Außenelektronen sagt. Beispielsweise steht das Element Chlor (Cl) in der siebten Hauptgruppe (Halogene). Demnach hat ein Chloratom sieben Valenzelektronen.Die Halogene sind sehr reaktionsfreudig. Das bedeutet, dass sie sehr gern und gut reagieren. Ursache ist, dass sie sieben Außenelektronen besitzen. Deshalb benötigen Halogene nur ein weiteres Elektron, um die Oktettregel zu erfüllen und eine Edelgaskonfiguration zu erreichen.Mit Ausnahme von Helium haben die Edelgase acht Außenelektronen auf ihrer äußersten Elektronenschale. Diesen Zustand bezeichnet man als Edelgaskonfiguration (höchst mögliche Anzahl an Außenelektronen). Helium hat zwei Außenelektronen, damit ist die erste Schale voll besetzt.
Was ist die 7 Hauptgruppe : Die Halogene stellen die 7. Hauptgruppe des Periodensystems dar. Zu ihnen gehören die Elemente Fluor, Chlor, Brom, Iod und das radioaktive Astat.
Welches Atom hat 7 Elektronen
Fluor hat sogar die höchste Reaktivität aller Elemente im Periodensystem. Sie können mit fast allen Elementen aus dem Periodensystem außer mit den Edelgasen (8. Hauptgruppe) Verbindungen eingehen. Das kommt daher, dass sie 7 Außenelektronen besitzen und ihnen 1 Außenelektron fehlt.
Wie viele Elektronen in der 7 Schale : Die äußerste (siebente) Elektronenschale, auch Valenzschale genannt, kann zwischen ein und acht Elektronen aufnehmen. Somit befinden sich insgesamt 32 chemische Elemente in der siebente Periode.
Eigenschaften des Elements
| Einordnung in das Periodensystem der Elemente und Eigenschaften | Atombau |
|---|---|
| Ordnungszahl: 76 | 76 Protonen 76 Elektronen |
| 6. Periode | 6 besetzte Elektronenschalen |
| VIII. Nebengruppe | 8 Außenelektronen |
| Elektronenkonfiguration im Grundzustand | Xe 6s24f1 45d6 |
Edelgase, mit Ausnahme des Heliums, haben acht Elektronen auf der Valenzschale. Diese Elektronenanordnung ist so stabil, dass die Edelgase nur schwer chemische Reaktionen eingehen. Vor allem treten die Edelgase im Gegensatz zu den anderen elementaren Gasen nicht als zweiatomige Moleküle auf.
Wie viele Elektronen sind in der 7 Schale
Die äußerste (siebente) Elektronenschale, auch Valenzschale genannt, kann zwischen ein und acht Elektronen aufnehmen. Somit befinden sich insgesamt 32 chemische Elemente in der siebente Periode.2,8Neon / Elektronen pro SchaleZusammenfassung. Die Elemente der VII. Hauptgruppe Fluor, Chlor, Brom und Jod faßt man unter dem Namen Halogene (Salzbildner, von ἂλς Δ̠ Salz) zusammen, weil sie sich unmittelbar mit Metallen zu Salzen, den Halogeniden, verbinden, von denen das Natriumchlorid, NaCl, als Kochsalz am längsten bekannt ist.
Halogene sind die Elemente der 7. Hauptgruppe des Periodensystems und gehören allesamt zu den Nichtmetallen. Zu der Gruppe der Halogene gehören Fluor (F), Chlor (Cl), Brom (Br), Iod (I), Astat (As) und das künstlich hergestellte, radioaktive Element Tenness.
Welches Element hat 7 Elektronen und 7 Protonen : Stickstoff
Ein Stickstoff-Atom besitzt 7 Protonen und 7 Elektronen.
Welches Atom hat 7 Protonen : Stickstoff ist ein Element der V. Hauptgruppe . Das Stickstoffatom besitzt 7 Protonen und meist 7 Neutronen im Atomkern sowie 7 Elektronen in der Atomhülle.
Wie viele Elektronen auf der äußeren Schale
erste Schale: K-Schale, Platz für 2 Elektronen. zweite Schale: L-Schale, Platz für 8 Elektronen. dritte Schale: M-Schale, Platz für 18 Elektronen. vierte Schale: N-Schale, Platz für 32 Elektronen.
2, 8, 14, 2Eisen / Elektronen pro SchaleEigenschaften des Elements
| Einordnung in das Periodensystem der Elemente und Eigenschaften | Atombau |
|---|---|
| 5. Periode | 5 besetzte Elektronenschalen |
| VIII. Nebengruppe | 9 Außenelektronen |
| Elektronenkonfiguration im Grundzustand | Kr 5s14d8 |
| Elektronegativität | 2,2 |
Wie viele Außenelektronen hat Indium : Eigenschaften des Elements
| Einordnung in das Periodensystem der Elemente und Eigenschaften | Atombau |
|---|---|
| Ordnungszahl: 49 | 49 Protonen 49 Elektronen |
| 5. Periode | 5 besetzte Elektronenschalen |
| III. Hauptgruppe | 3 Außenelektronen |
| Elektronenkonfiguration im Grundzustand | Kr 5s24d1 05p1 |