Calciumcarbonat (fachsprachlich), auch Kalziumkarbonat oder veraltet kohlensaurer Kalk, ist eine chemische Verbindung mit der chemischen Formel CaCO3. Es ist ein Calcium-Salz der Kohlensäure (Carbonat) und besteht im festen Zustand aus einem Ionengitter mit Ca2+-Ionen und CO32–Ionen im Verhältnis 1:1.Kalk, bzw. Calciumcarbonat ist ein Salz der Kohlensäure. Viele Gebirge wie die Schwäbische Alb, die Kreidefelsen in Rügen oder die Dolomiten bestehen hauptsächlich aus Kalk. Häufig finden sich dort Versteinerungen von ehemaligen Meerestieren.Calciumcarbonat ist eine Base, welche die Magensäure neutralisiert.
Ist CaCo3 wasserlöslich : Calciumcarbonat selbst ist in reinem Wasser kaum löslich. Die Löslichkeit beträgt gerade einmal 14 Milligramm pro Liter, wobei das Carbonat-Ion als Hydrogencarbonat-Ion in Lösung geht.
Ist calciumacetat ein Salz
Calciumacetat (auch essigsaurer Kalk) (E 263) ist eine chemische Verbindung mit der chemischen Formel Ca(CH3COO)2. Es ist ein Calcium-Salz der Essigsäure. Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen.
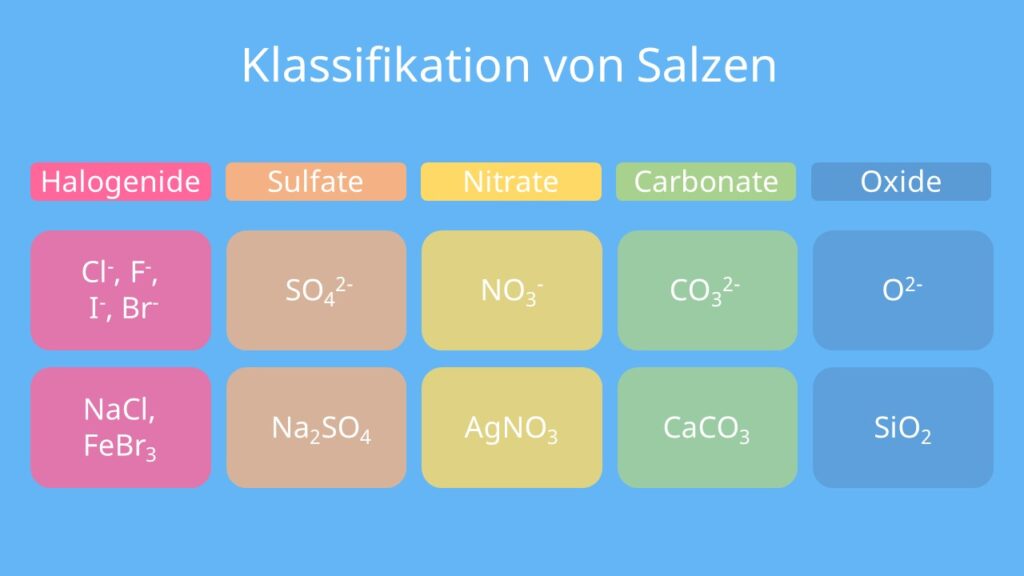
Welche Salze gibt es in der Chemie : Salze Chemie Liste
| Säure | Name ihrer Salze | Beispiel |
|---|---|---|
| Phosphorsäure | Phosphate | Natriumphosphat (Na3PO4) |
| Salzsäure | Chloride | Natriumchlorid (NaCl) |
| Salpetersäure | Nitrate | Silbernitrat (AgNO3) |
| Schwefelsäure | Sulfate | Calciumsulfat (CaSO4) |
CaCO3 ist eine Summenformel, die ein weißes oder transparentes kristallförmiges Mineral beschreibt. Calciumcarbonat (gewohnheitsmäßiger Name – Calcit) besteht aus den Salzen von Kohlensäure und Kalzium.
Carbonate sind ionische Salze und deshalb bei Raumtemperatur in der Regel kristalline Feststoffe. Das Carbonat-Anion bringt keine Eigenfarbe in die Verbindungen ein, so dass deren Farbe ggf. durch das betreffende Kation bestimmt wird. Carbonate sind geruchlos.
Was ist CaCO3 Chemie
Lexikon der Chemie Calciumcarbonat. Calciumcarbonat, veraltet kohlensaurer Kalk, CaCO3, bildet drei Modifikationen: den trigonalen Calcit (Kalkspat), den rhombischen Aragonit und den hexagonalen Valerit.Lexikon der Chemie Calciumcarbonat. Calciumcarbonat, veraltet kohlensaurer Kalk, CaCO3, bildet drei Modifikationen: den trigonalen Calcit (Kalkspat), den rhombischen Aragonit und den hexagonalen Valerit.Eigenschaften
Calciumcarbonat ist ein weißer, farb- und geruchloser Feststoff, der in Säuren unter Entwicklung von Kohlendioxid gut löslich ist. In organischen Lösungsmitteln ist es unlöslich, in Wasser nahezu unlöslich. Die Verbindung kommt in wasserfreien Formen, als Hydrat sowie in amorphen Formen vor.
Calciumnitrat ist das Calciumsalz der Salpetersäure und hat die Summenformel Ca(NO3)2. „Kalk- oder Norgesalpeter“ wird als Düngemittel verwendet.
Ist natriumacetat ein Salz : ist das Natriumsalz der Essigsäure und wird durch die Reaktion von Essigsäure mit einer Natriumverbindung gewonnen. Es ist ein farbloses Salz mit schwachem Essiggeruch, das gut in Wasser aber nur schlecht in Alkohol löslich ist. Wenn eine gesättigte Natriumacetatlösung kristallisiert, entsteht Hitze.
Welche Stoffe sind Salz : Zu den Salzen zählen zum Beispiel die Carbonate, die Chloride, die Nitrate, die Phosphate oder die Sulfate. Sie kommen in der Natur in großer Zahl in den Mineralien vor und bilden oft schön ausgeformte Kristalle. Steinsalz ist aus Natriumchlorid aufgebaut. Gips besteht aus Calciumsulfat Dihydrat.
Was sind Salze Beispiele
Salze Chemie Liste
| Säure | Name ihrer Salze | Beispiel |
|---|---|---|
| Flusssäure | Fluoride | Calciumfluorid (CaF2) |
| Phosphorsäure | Phosphate | Natriumphosphat (Na3PO4) |
| Salzsäure | Chloride | Natriumchlorid (NaCl) |
| Salpetersäure | Nitrate | Silbernitrat (AgNO3) |
Calciumcarbonat (auch Kalk genannt, chemische Formel CaCo3) ist ein Salz der Kohlensäure. Es handelt sich um einen Stoff, der zu den häufigsten auf der Erde zählt. Calciumcarbonat steckt beispielsweise im Mineral Calcit sowie in unseren Knochen und Zähnen.Calciumcarbonat ist eine anorganische Verbindung, die in Privathaushalten und in der Industrie sehr weit verbreitet ist. Dieser natürliche Rohstoff ist auch als Calcit oder Salz von Kohlensäure und Kalzium bekannt.
Wie nennt man die Salze der Kohlensäure : Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Kohlensäure (H2CO3) ist eine Säure und das Reaktionsprodukt von Kohlenstoffdioxid (CO2) mit Wasser. Die Salze der zweiprotonigen Säure heißen Carbonate bzw. Hydrogencarbonate, auch ihre Ester werden Carbonate genannt.